摘要
研究了氢氧根和氟离子与铝离子(γOH 和 γF)的摩尔比对混凝和电混凝(EC)的影响,以解决酸或碱过量添加的问题。当 γOH 和 γF(γOH+F)之和接近3时,除氟效率大约为100%。这一发现表明,氟离子和氢氧根离子可以与铝离子共沉淀,沉淀物的公式为 AlnFm(OH)3n-m。然而,当 γOH 小于2.4时,除氟效率在 γOH+F=3 的条件下随着 γOH 的下降而下降,因为形成的铝聚合物量减少。当 γOH+F>3时,EC的除氟效率超过了相同 γOH 和 γOH+F 的混凝效率,证明了电凝聚效应的存在。
1引言
去除氟化物对环境工程来说一直非常重要,因为在半导体行业中使用了大量氢氟酸。长期以来,人们一直使用铝盐混凝来去除氟离子。当Al(III)离子被添加到含氟化物的水中时,可能会发生共沉淀或吸附。使用固定量的铝盐去除氟化物的效率取决于pH值、碱度、共存阴离子以及溶液的其他特性。最适合混凝除氟的pH值为5.5-6.5。预先确定在除氟过程中添加到溶液中的酸或碱的量以确定理想的pH值是困难的,因为这个范围内的pH值对酸或碱的浓度非常敏感。此外,由于氟离子与铝离子(Al(III))或被氢氧化铝吸收,溶液的pH值会发生变化,因为氢氧根离子从氢氧化铝中释放出来。因此,所测量的pH值可能并不是反应完全时的pH值。因此,在实际操作中,酸或碱常常被过量添加氢氧根离子的初始浓度和铝离子(Al(III))的量会影响溶液的pH值。如果以氢氧根离子与铝离子(OH⁻/Al³⁺)的初始摩尔比(γOH,γOH=[OH⁻]/[Al³⁺])来确定除氟效率的关系,那么过量添加酸和碱的问题就可以得到解决。此外,由于氢氧化铝除氟会导致氢氧根离子的释放,因此还应考虑除氟效率与溶液中氟离子(F⁻)与铝离子(Al³⁺)的初始摩尔比(γF,γF=[F⁻]/[Al³⁺])之间的关系。
使用铝电极的电混凝是一种新的除氟方法。当电流通过铝电极时,阳极反应会释放出铝离子(Al(III)),这些铝离子随后与阴极产生的氢氧根离子以及氟离子发生反应:
Al(s) → Al³⁺(aq) + 3e⁻ (1)
2H₂O(l) + 2e⁻ → 2OH⁻(aq) + H₂(g) (2)
有学者指出,由于电凝聚作用,电凝聚系统(EC)的除氟效率可能超过传统凝聚过程。氟离子被吸引到阳极,因此阳极附近的氟浓度超过了溶液主体中的浓度。因此,电凝聚的除氟效率应该高于凝聚。然而,有学者人并未进行任何实验来比较电凝聚与传统凝聚。因此,这一推论尚未得到证实。
据报道,较低的初始pH值可以提高电凝聚过程中除氟的效率,但由于系统的最终pH值变化很小(因为Al(III)离子是缓冲物种),所以改善并不显著。有学者证明,电凝聚中的最终pH值约为6。如果在电凝聚中不量化初始γOH和γF对除氟的影响,也可能会发生过载问题。通过控制初始γOH来控制除氟效率比通过控制初始pH更为方便,因为可以预先确定添加的酸或碱的量。
本研究调查了γOH和γF对凝聚和电凝聚系统中除氟的影响,并比较了两种系统的除氟效率,以证明电凝聚效应的存在。
2材料与方法
2.1.混凝
使用氟化钠(NaF)、氢氧化钠(NaOH)和硝酸铝(Al(NO₃)₃)盐分别制备了Al³⁺、OH⁻和F⁻离子的储备溶液,溶解于蒸馏水中。将预定量的Al³⁺和F⁻离子储备溶液加入到50毫升的容量瓶中,并向另一个50毫升的容量瓶中加入OH⁻的储备溶液。然后将两种溶液分别稀释至50毫升,并在塑料瓶中混合。在150转/分钟和25°C的条件下,使用摇床(Yihder,BT-350R)持续摇晃瓶子。24小时后提取样品,并通过孔径为0.2微米的Millipore滤器(MES,直径25mm)进行过滤。使用pH电极和专用氟电极分别测定过滤水中的pH值和氟浓度。沉淀物通过固态核磁共振(Bruker,DSX-300 NMR)在8 kHz频率下进行分析。
2.2.电混凝
实验在双极批处理反应器中进行,反应器中有七个铝电极并联,有学者所使用。只有外部电极连接到电源,当电流通过电极时,阳极和阴极反应发生在内部电极的每个表面上。通过电极传递的电流。每批溶液的体积(V)为11升。除外部电极外,每个电极的有效面积为8×9cm,外部电极的尺寸减小以防止电场的分散。因此,每批的面积/体积比为40.9m-1—高于一些学者报告的所需值。每对电极之间的距离为1厘米。使用恒电位仪在恒流模式下保持恒定电流。外部电极的电流密度为8.16×10-3安培/平方厘米,内部电极为5.56×10-3安培/平方厘米。在400转/分钟的磁力搅拌下,保持批处理反应器中溶液的均匀性。每个系统的温度保持在25±1°C。
样品每分钟提取一次,然后立即通过0.2微米混合纤维素酯膜过滤。每个样品中残留的氟化物浓度([F⁻]res),包括最终氟化物浓度([F⁻]f),使用离子色谱仪(Dionex,DX-100)测定。每个系统中氟化物的初始浓度([F⁻]0)为25mg/L。以下方程定义了每批除氟效率:
εF=1-[F⁻]f/[F⁻]0 (3)
每次反应后,使用原子吸收光谱光度计(标准方法,第3030节)测量从消化样品中获得的Al(III)的总浓度。从而确定了Al(III)的用量([Al³⁺]T)。根据法拉第定律,理论Al(III)的用量([Al³⁺]theo)可以计算为:
[Al3+]theo=nIT/VZF,Z=3for Al(III) (4)
其中n是电池数量,I是电流,T是反应的保留时间,V是溶液体积,Z是铝的价数,F是法拉第常数(F=96487)。
电凝聚后从消化样品中获得的Al(III)用量与理论Al(III)用量的比率被定义为电效率(εc):
εc=[Al3+]T/[Al3+]theo (5)
在电凝聚反应过程中某一时刻的Al(III)用量([Al³⁺]t)可以按如下估算:
[Al3+]t=εcnIt/VZF, Z=3for Al(III) (6)
如果在电凝聚过程中初始溶液中没有碱或酸存在,则γOH为3,因为当电流通过电极时产生的Al(III)和氢氧根离子的量是化学计量等价的(方程(1)和(2))。可以通过改变初始酸度([H⁺]0)或碱度([OH⁻]0)来调整电凝聚系统中的最终γOH,如下所示:
γOH=3+[OH⁻]0/[Al3+]t-[H⁺]0/[Al3+]t (7)
本研究中凝聚实验的铝用量范围为1至5 mM。方程(6)中的εc范围为1至5 mM。在本研究中,由于电极腐蚀条件的变化,范围从1.2到1.3。根据方程(6),当[Al]为5 mM且εc为1.2时,T为8.34分钟。为了比较电凝聚(EC)与凝聚实验的结果,选择了9分钟的反应时间。
所有分析均进行了重复实验以确保数据的可重复性,图表和表格中的所有数据均为平均值。
3结果与讨论
3.1.混凝
图1 描绘了不同初始铝剂量下剩余氟化物浓度与γOH的关系。随着γF的增加,γOH下降。γOH和γF(γOH+F)之和似乎保持不变。因此,研究了剩余氟化物浓度随γOH+F的变化,使用不同的初始Al(III)剂量,如图2所示。如果初始铝剂量大于1 mM,γOH+F接近3。图2还显示,当γOH+F超过3时,剩余氟化物浓度迅速上升。Al(OH)₃沉淀中氢氧根离子与Al(III)离子的摩尔比为3。因此,氟离子和氢氧根离子可以与Al(III)离子共沉淀形成AlₙFₘ(OH)3n-m:
nAl3+(aq)+(3n-m)OH-(aq)+mF-(aq)→AlnFm(OH)3n-m(s) (8)
然而,当γOH+F超过3时,沉淀中的氟离子很容易被氢氧根离子替代:
AlnFm(OH)3n-m(s)+OH-(aq)→AlnFm-1(OH)3n-m+1(s)+F-(aq) (9)
氢氧根离子对Al(III)的亲和力比氟离子大。因此,氟离子只有在与Al(III)离子配位时才被氢氧根离子替代。如果氢氧根离子的量不足以中和Al(III)的正电荷,氟离子就会替代氢氧根离子。
图3 描绘了pH与γOH的关系,有和没有氟化物存在时氟化物在混凝过程中的存在。两个系统测量的pH值仅在γOH=2.5-3的范围内有所不同。除了该范围外,两个系统的pH值几乎相同。在含氟系统中,pH在γOH=2.5时迅速上升,但在不含氟系统中,pH在γOH=2.8时上升,验证了氟化物是氢氧根离子的替代离子。此外,除氟的pH值在含氟曲线的拐点处,这解释了为什么系统中的pH值如此难以达到。
OH⁻的浓度可以被视为这些实验中水的碱度。然而,天然水的碱度主要是由弱酸盐的溶解引起的,如碳酸盐或碳酸氢盐。因此,使用碳酸盐来研究Al(III)与碱度的摩尔比对从天然水中去除氟化物的影响。Al(III)与碳酸盐的双摩尔比定义为γAlk(γAlk = 2[CO₃²⁻]/[Al³⁺])并且γAlk和γF的总和定义为γAlk+F。
如图所示在图4中的γAlk+F也接近3,但随着γAlk+F的增加,氟化物的剩余浓度上升速度比使用氢氧化铝系统中慢,因为在γAlk+F超过3时,形成了碳酸氢盐(HCO₃⁻)而不是氢氧根。碳酸氢氧化铝(Al(III))对碳酸盐的亲和力小于氟化物。因此,随着γAlk+F的增加,氟化物的剩余浓度上升非常缓慢。
图1
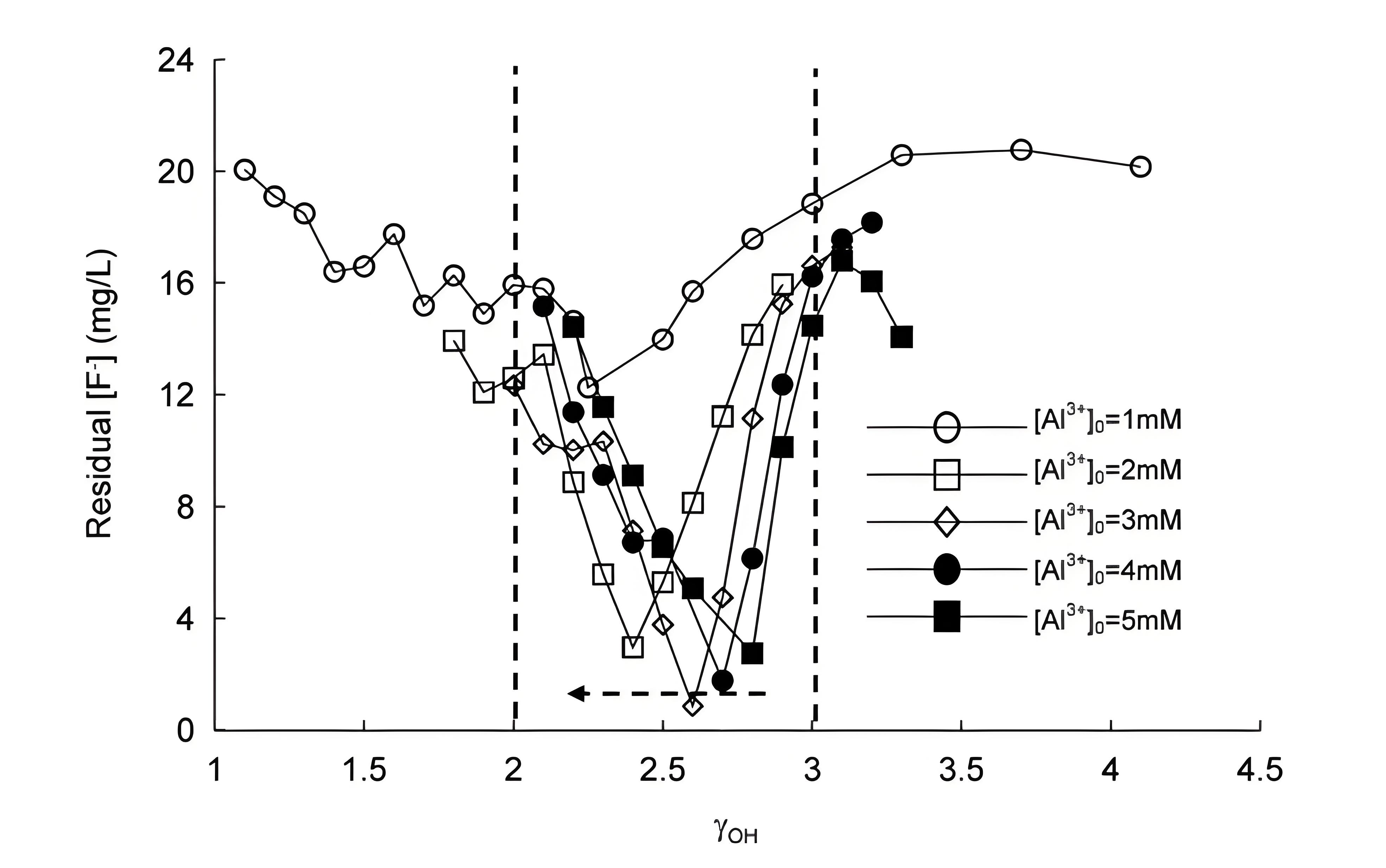
图1.不同铝剂量下剩余氟化物浓度随γOH的变化。γOH随着[Al³⁺]₀的减少而下降。由于所有系统中初始氟化物浓度恒定([F⁻]₀=25 mg/l),随着[Al³⁺]的减少,γF增加。
图2

图2.不同铝剂量下剩余氟化物浓度随γOH+F的变化([F⁻]₀=25 mg/L)。
图3

图3. 在有无氟化物离子的情况下,pH值随γOH变化的情况([Al³⁺] = 3 mM,[F⁻]₀ = 25 mg/L)。
图4

图4. 在混凝过程中,使用碳酸钠(Na₂CO₃作为碱性物质时,剩余氟化物浓度随γAlk+F的变化([Al³⁺] = 3 mM,[F⁻]₀ = 25 mg/L)。
图5

图5. 在电凝聚(EC)过程和混凝系统(混凝)中,剩余氟化物浓度随γOH+F的变化。([Al³⁺] = 3 mM,[F⁻]₀ = 25 mg/L)。
3.2. 电凝聚(EC)
图5比较了电凝聚(EC)与混凝过程中剩余氟化物浓度的变化。混凝实验结果表明,如果γOH超过3,除氟效率几乎为零。因此,仅考虑了γOH<3范围内的变化。EC系统的γOH+F也接近3。此外,如果γOH+F>3,EC系统中的剩余氟化物浓度低于混凝系统中的浓度,证明了电凝聚效应的存在。
图6

图6. 在电凝聚(EC)和混凝过程中,随着γOH的变化,除氟效率的变化,γOH+F = 3 ([F⁻]₀ = 25 mg/L)。
根据方程(7),电凝聚(EC)系统中的γOH+F可以按如下计算:
γOH+F = 3 + [OH⁻]₀/[Al³⁺]t - [H⁺]₀/[Al³⁺]t + [F-]₀/[Al³⁺]t (10)
如果初始碱度为零且初始酸度等于初始氟化物浓度([H⁺]₀ = [F⁻]₀),那么γOH+F与Al(III)剂量无关,并且在EC反应过程中始终等于3。如前所述,Al(III)剂量与EC中的反应时间成正比,如方程(8)所示。因此,可以通过测量EC系统中不同保留时间的氟化物浓度来建立γOH+F = 3时剩余氟化物浓度与Al(III)剂量之间的关系。图2显示,当初始铝剂量为1 mM时,γOH+F超过3,该系统中的除氟效率远低于其他系统。因此,当γOH+F = 3时,需要最小Al(III)剂量以在混凝中保持高效率。由于γOH+F = 3时,EC和混凝的εF非常接近,因此可以采用EC来寻找混凝中的最小γOH。环境工程师使用EC来确定最小γOH比使用混凝更方便、更快。γOH随EC中的反应时间变化,因此只需要一个EC过程来确定γOH。然而,如果γOH由混凝确定,则必须进行许多实验。
图7

图7. 在OH/Al比为2.4(γOH+F = 3)时的铝氟化铝的固态核磁共振(NMR)光谱以及氢氧化铝。
图6显示了当γOH+F = 3时,混凝和电凝聚(EC)过程中的剩余氟化物浓度与γOH的关系。当γOH ≥ 2.4时,εF 几乎达到100%,并且随着γOH在两种系统中的下降而下降。这种现象表明,氢氧离子与Al(III)离子在氟化铝沉淀物中的摩尔比应超过一定限度以保持沉淀稳定。因此,Al(III)离子与氢氧离子和氟离子共沉淀的同步应形成氢氧化铝聚合物。当γOH小于2.46时,如果氢氧化铝聚合物与总铝剂量的比例小于2.46,则形成氢氧化铝聚合物。是一个线性函数,如下所示:
[Alₚ]/[Al³⁺]ₜ = γOH/2.46,for γOH < 2.46. (11)
添加对Al(III)具有高亲和力的阴离子,如硫酸根、磷酸根和硅酸根,会导致聚合物因聚合物之间的静电排斥力减少而迅速聚集。有报告称,添加氟离子也会导致聚合物的快速沉淀。因此,去除的氟离子应与氢氧化铝聚合物的形成量成正比。因此,如图6所示,如果γOH < 2.4,εF与γOH成正比,如果γOH > 2.4,则接近100%。上述推断还解释了为什么当γOH+F < 3时,EC和混凝过程中的氟去除效率几乎相同。由于当γOH+F < 3时,氟化物去除效率主要由氢氧化铝聚合物的量控制,因此由于电凝聚效应导致的氟化物浓度增加不能提高氟去除效率。因此,尽管当γOH+F < 3时也发生了电凝聚效应,但氟去除效率并未提高。
核磁共振(NMR)可以用来确定“笼状”Al 13聚合物。图7展示了在OH/Al比为2.4时铝氟化物沉淀物和氢氧化铝的27Al NMR光谱。在62.5 ppm处有一个明显的峰值,这是OH/Al比为2.4时沉淀物中Al 13聚合物的峰值,但在铝氢氧化物光谱中没有62.5的峰值。这一事实表明,在OH/Al比为2.4时铝氟化物沉淀物中存在“笼状”Al 13聚合物。然而,根据Al³⁺浓度和碱度、搅拌强度、温度、碱注入速率和老化时间的不同,各种Al聚合物种类在部分中和Al³⁺溶液中形成。不稳定的聚合物种类需要1-5天才能通过NMR检测不到,自组装成“笼状”Al 13聚合物。在这项研究中的老化时间不到5分钟。因此,在OH/Al比为2.4时制备的沉淀中可能存在其他氢氧化铝聚合物种类。
4. 结论
γOH和γF控制铝盐的除氟化物去除。混凝和电凝聚过程中除氟的γOH+F接近3,如果γOH超过2.4。当γOH+F超过3时,随着γOH的增加,除氟效率迅速下降。如果γOH小于2.4,当γOH+F为3时,随着γOH的下降,除氟效率下降,因为形成的铝聚合物量减少。电凝聚过程中的除氟效率超过混凝过程,对于相同的γOH+F和γOH+F,当γOH+F超过3时,这是由于电凝聚效应。使用γOH或γAlk比使用pH更方便,以在混凝或EC系统中修正εF。通过精确测量处理水中的碱度、酸度和氟化物浓度可以解决过量添加酸或碱的问题。